5月13日,药学院刘彬&吉敬课题组团队再次以江苏海洋大学为论文第一完成单位和通讯单位在Nature(《自然》)旗下知名刊物Cell Death and Disease(IF=9,中科院1区,TOP期刊)上发表高水平文章。此次论文题目为:FOXP4-mediated induction of PTK7 activates the Wnt/β-catenin pathway and promotes ovarian cancer development。该论文首次揭示了FOXP4在Wnt信号通路和卵巢癌发生发展中的关键调控作用,为卵巢癌靶向治疗提供了新的重要理论依据。药学院的吉敬副教授是该文第一作者,刘彬教授、刘伟教授为共同通讯作者。

FOXP4在卵巢癌中显著上调,与不良预后相关。通过TCGA和GTEx数据分析,发现FOXP4 mRNA在6种癌症特别是卵巢癌组织中显著上调。临床样本发现晚期卵巢癌患者FOXP4 mRNA表达水平高于早期患者。此外,单细胞测序结果表明FOXP4主要在恶性肿瘤细胞中高表达,而在间质细胞和免疫细胞中表达较低。Kaplan-Meier Plotter分析表明FOXP4高表达患者总生存率和无进展生存率较低,揭示了FOXP4在卵巢癌中的潜在临床价值。
FOXP4是Wnt/β-catenin/TCF4信号通路的转录靶点。该团队进一步通过TCGA数据库分析显示FOXP4与Wnt/β-catenin信号通路激活密切相关,且与多个Wnt相关基因呈强相关。LiCl和β-catenin过表达均增加FOXP4表达,而ICG-001或CTNNB1沉默则减少其表达。JASPAR数据库发现FOXP4启动子区域存在两个潜在TCF4响应元件,Chip验证进一步证实TCF4与FOXP4结合。FOXP4敲除抑制了卵巢癌细胞增殖和克隆形成,降低了迁移和侵袭能力,且体内研究证实FOXP4的沉默显著减小了裸鼠移植瘤的大小。这些结果表明FOXP4在卵巢癌发展中扮演重要角色。
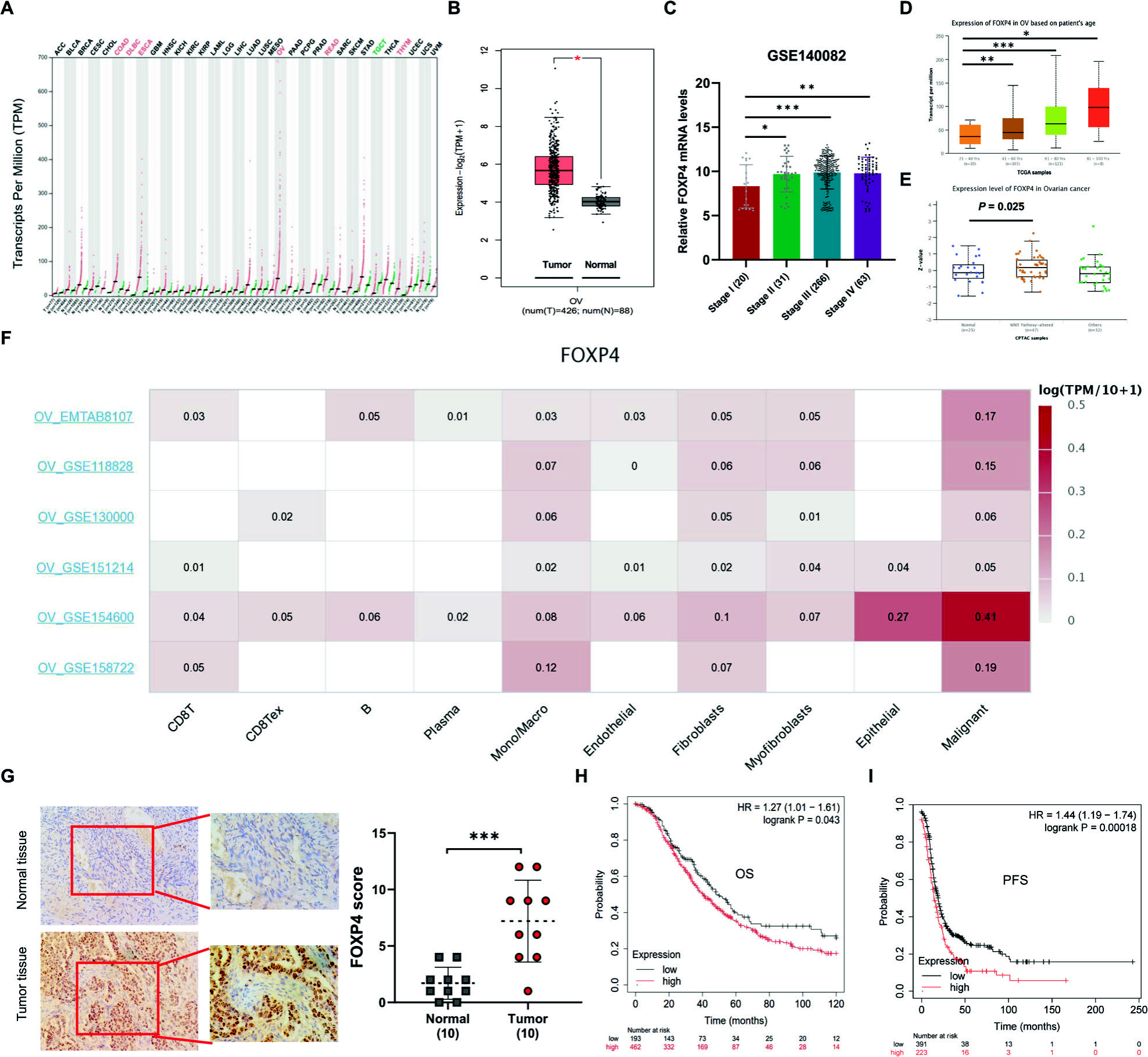
图1 FOXP4上调与卵巢癌症患者预后不良相关
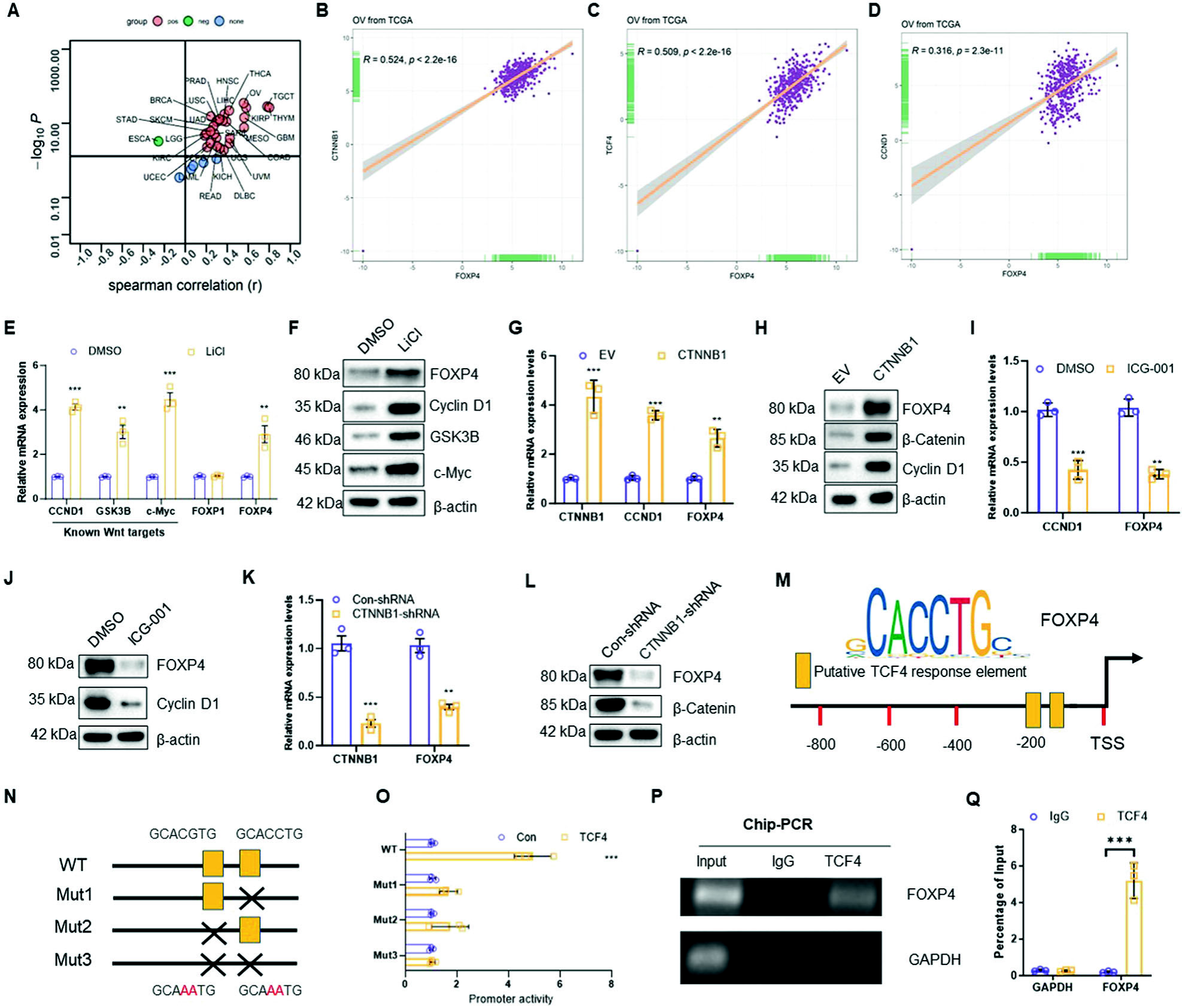
图2 FOXP4是Wnt/β-catenin/TCF4信号通路的转录靶点
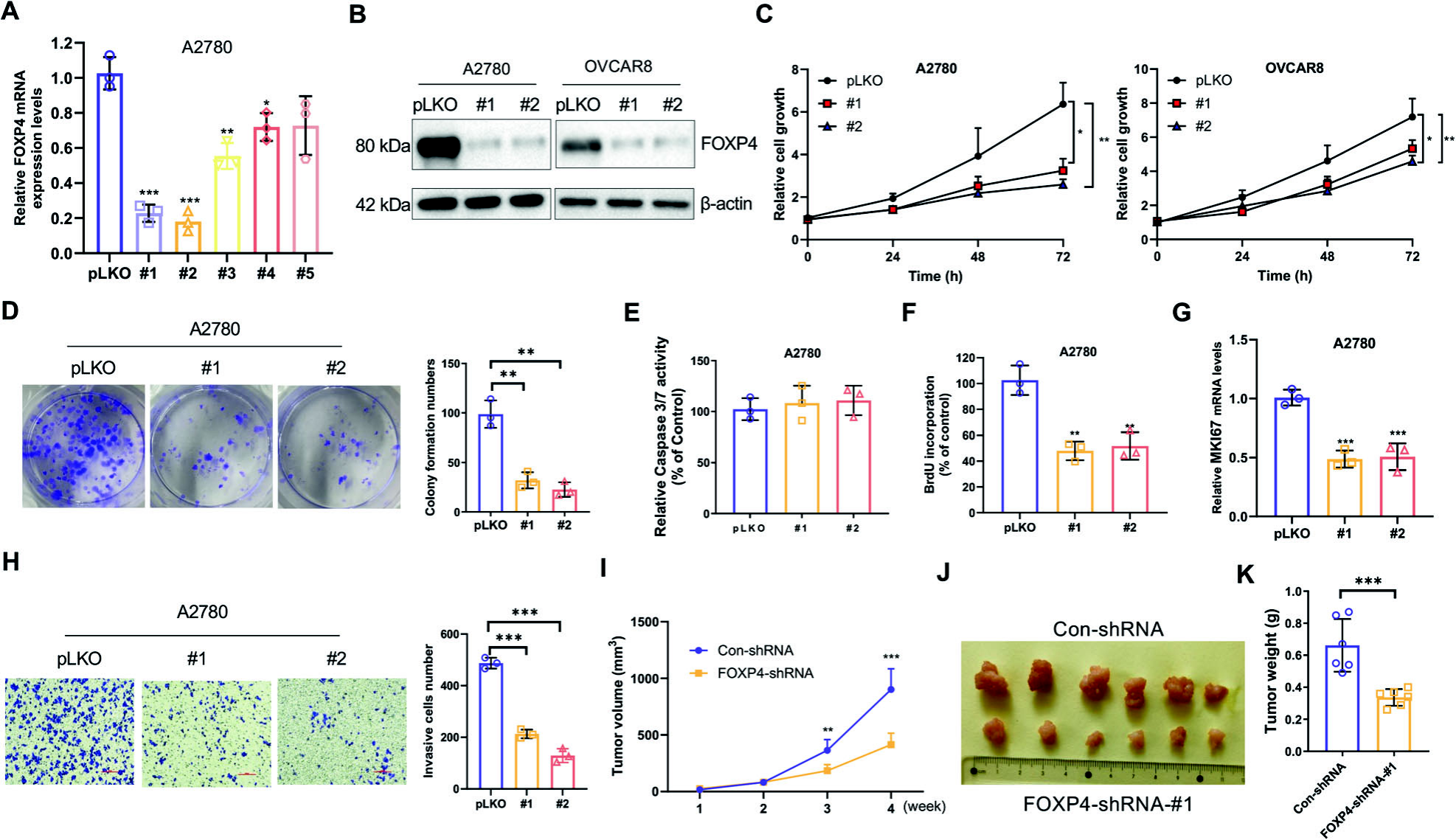
图3 OV恶性肿瘤细胞的发育需要FOXP4
该团队通过CRISPR-Cas9技术制备FOXP4敲除细胞系,RNA测序结果显示FOXP4 KO细胞中Wnt/β-catenin信号通路显著下调。TCGA数据库分析表明FOXP4高表达组富集Wnt/β-catenin信号通路。沉默FOXP4降低TCF/LEF1荧光素酶活性及其下游靶基因转录,相应蛋白表达也减少。而FOXP4过表达则增加这些基因的表达,ICG-001抑制了这一效应,揭示了FOXP4对Wnt/β-catenin信号通路的激活在卵巢癌中至关重要。
通过分析TCGA卵巢癌数据库中与FOXP4共表达的基因,发现PTK7与FOXP4在卵巢癌和其他癌症类型中呈显著相关性。通过FOXP4的过表达和沉默实验证明,FOXP4可以直接调节PTK7的转录和蛋白表达。利用JASPAR在线数据库,我们发现PTK7启动子区域存在FOXP4的响应元件,表明FOXP4可能作为转录因子诱导PTK7的转录。这些结果揭示了FOXP4通过直接调节PTK7的表达来增强Wnt/β-连接蛋白信号通路的活性。
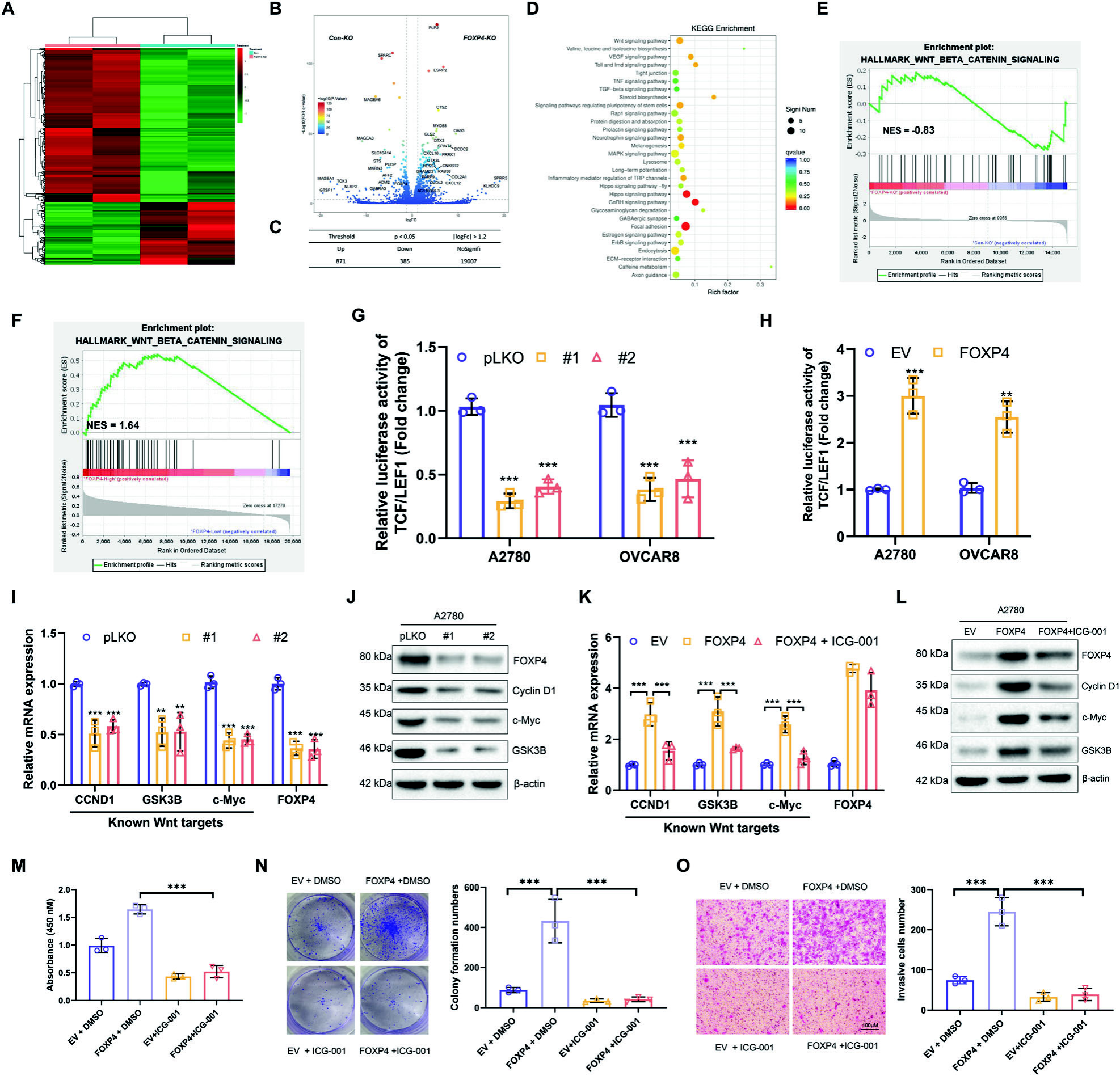
图4 FOXP4在OV中作为Wnt/β-catenin信号通路的正调控因子
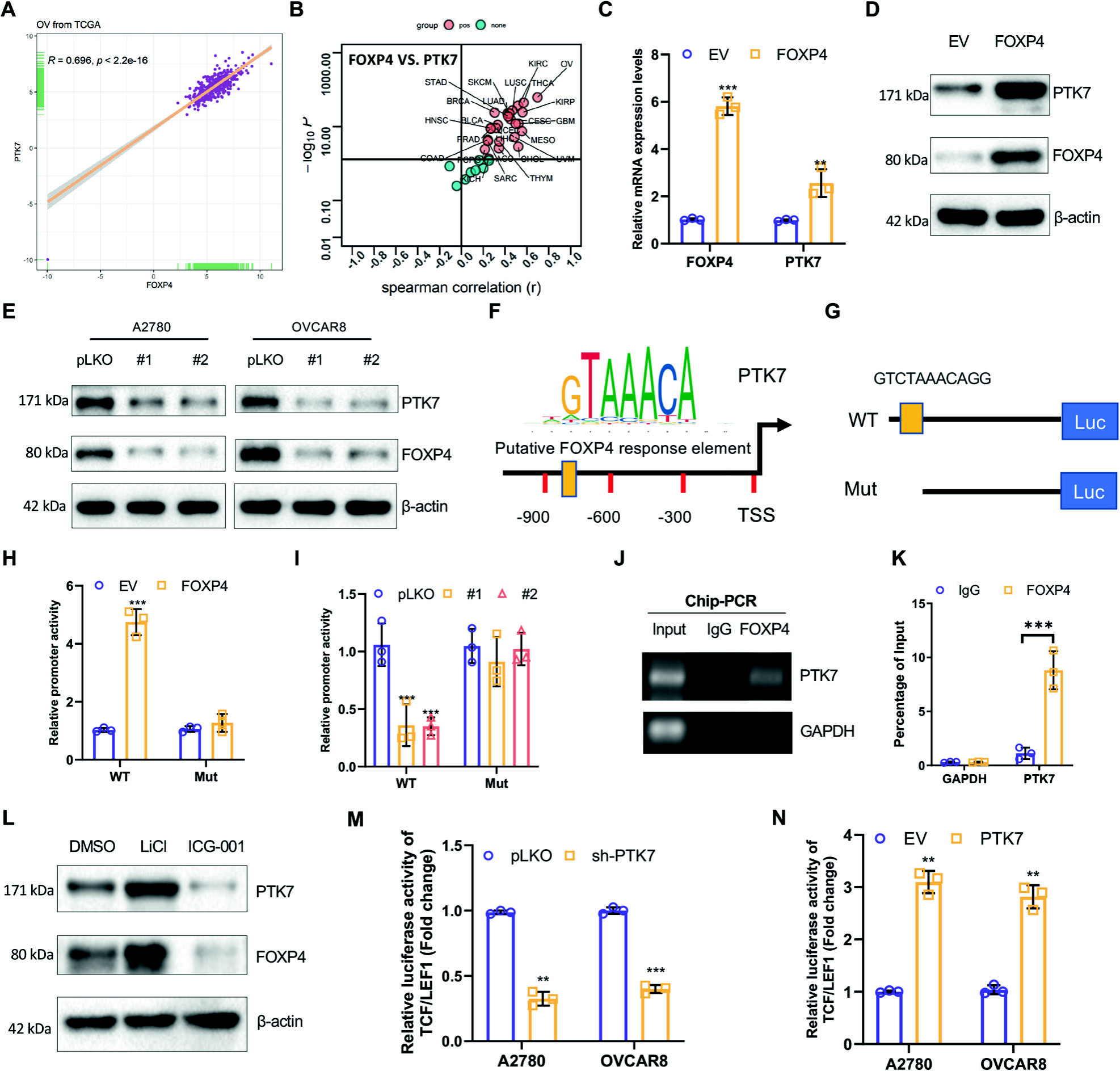
图5 PTK7是OV中FOXP4的转录靶标
该团队通过稳定表达外源PTK7的FOXP4敲除细胞,证明了PTK7在FOXP4介导的卵巢癌促肿瘤功能中的作用,并观察到PTK7过表达能够部分逆转FOXP4敲除对卵巢癌细胞增殖、集落形成和侵袭能力的影响。随后,创建了稳定过表达FOXP4并同时沉默PTK7的卵巢癌细胞,发现PTK7的沉默阻碍了FOXP4过表达引发的细胞恶性行为,并在小鼠异种移植瘤模型中验证了这一观察结果。综上所述,这些结果表明PTK7在促进FOXP4在卵巢癌细胞中的肿瘤促进效应中起关键作用,突显了在此背景下抑制PTK7的重要性。
本次研究成果原创性的发现FOXP4在卵巢癌中的功能和具体分子机制,为卵巢癌提供新的治疗靶点,为新型药物的开发和患者的治疗带来新希望。此研究获得国家自然科学基金项目、江苏省杰出青年基金项目、江苏省高校自然科学基金重大项目、江苏省高校“青蓝工程”骨干教师建设项目经费等的资助。
该课题组自组建以来,紧紧围绕临床癌症重大疾病治疗的信号通路和新靶点,采用独创性的药物靶向蛋白质降解新技术研究手段,对乳腺癌、结肠癌和卵巢癌等系列癌症的信号通路和治疗靶点进行深入研究,取得了一系列标志性科研成果,在该领域研究达到了国内外领先水平,有效提高了我校药学学科的科研水平和学术影响力。药学院高水平论文持续产出,是学校有组织引育高水平人才和学院积极开展有组织科研的结果。药学院将进一步加大对高水平科研成果的支持力度,整合校内外资源,助推更多高水平、高质量科研成果产出,为学校高质量内涵式发展奠定坚实基础。
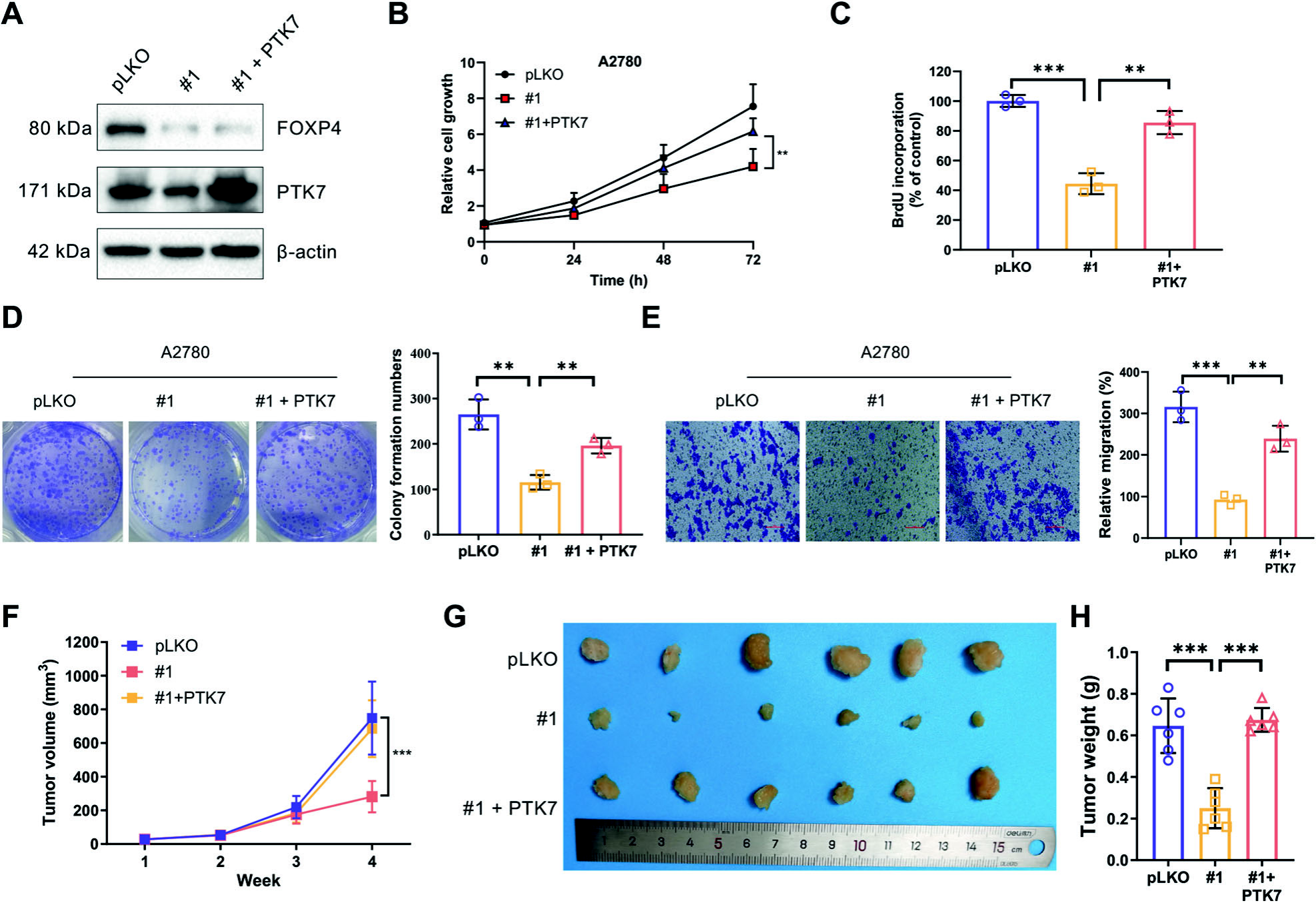
图6 FOXP4在OV细胞中的致癌潜力需要PTK7
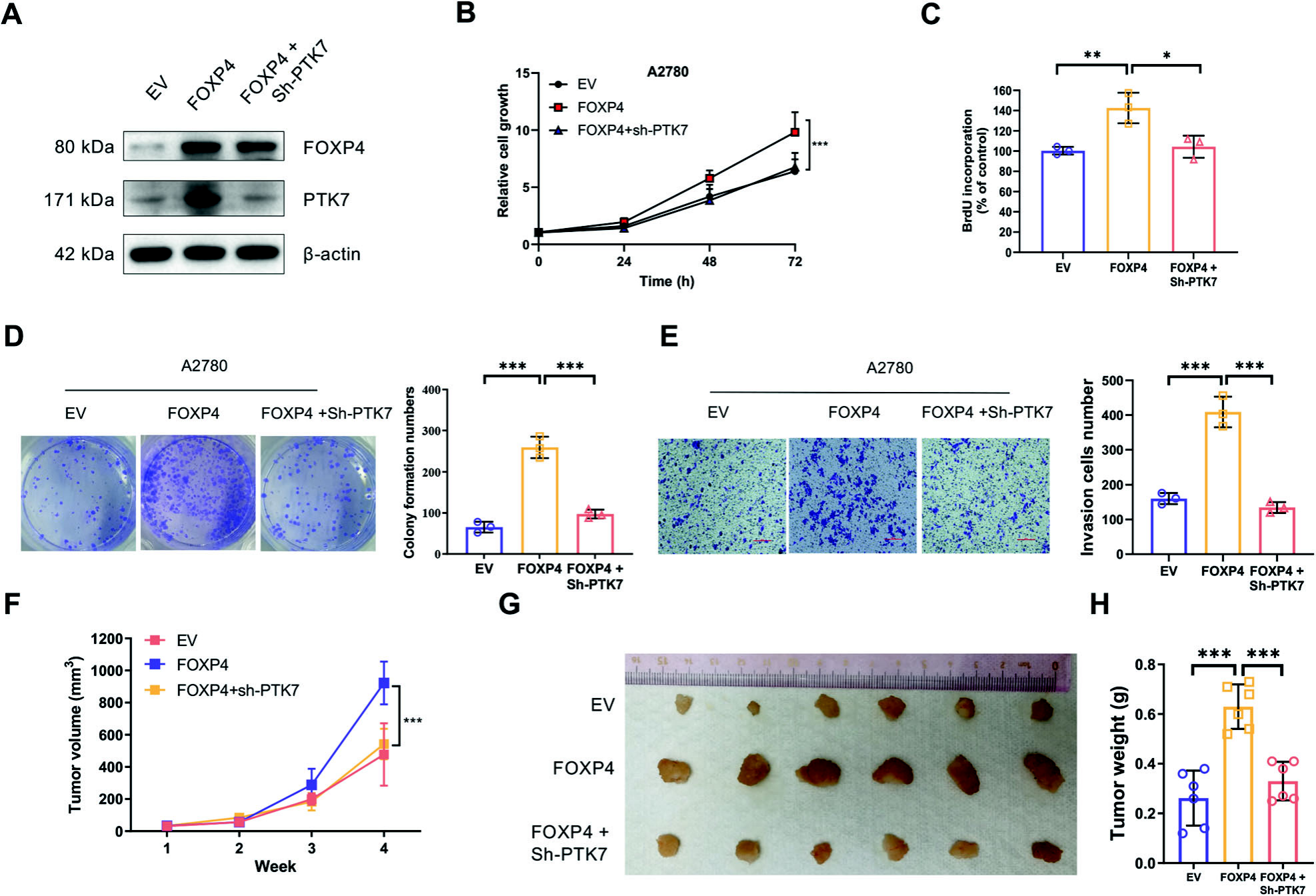
图7 FOXP4稳定过表达和PTK7同时沉默的OV细胞
全文链接:https://www.nature.com/articles/s41419-024-06713-7